Cáncer Gástrico
En este post encontraras información científica detallada referente al estudio y tratamiento del cáncer gástrico en todas sus etapas.
Apunte Resumen para alumnos de pregrado.
Clase de filtraciones post gastrectomía total (NUEVO)
Generalidades en Cáncer Gástrico
En esta sección podrás descargar artículos de revisión referentes a aspectos generales de la epidemiología, factores de riesgo, diagnóstico y tratamiento del cáncer gástrico.
- Situación del cáncer gástrico mundial y en Chile
http://www.sciencedirect.com/science/article/pii/S0379389316301533
- Evolución del cáncer gástrico en los últimos 40 años
http://www.scielo.cl/scielo.php?script=sci_arttext&pid=S0034-98872006000400004
- Morbilidad y mortalidad en gastrectomía oncológica
http://www.scielo.cl/scielo.php?script=sci_arttext&pid=S0718-40262011000600007
- Evolución en 44 años de cáncer gástrico incipiente
http://www.scielo.cl/scielo.php?script=sci_arttext&pid=S0718-40262015000200010
- Sobrevida de ca gástrico IIIC y IV
http://www.scielo.cl/scielo.php?script=sci_arttext&pid=S0718-40262014000500009
- Cirugía de cáncer gástrico y esofágico en edad avanzada
https://www.ncbi.nlm.nih.gov/pubmed/26303645
- Resumen estudio y tratamiento cáncer gástrico CLC
http://www.sciencedirect.com/science/article/pii/S0716864013702013
- Pronóstico stroma tumoral ratio Nuevo
https://www.ncbi.nlm.nih.gov/pubmed/28629870
- Factores pronósticos de sobrevida alejada en cáncer gástrico Nuevo
http://www.revistacirugia.cl/index.php/revistacirugia/article/view/170/58
- Cáncer gástrico en octogenarios Nuevo
http://www.sciencedirect.com/science/article/pii/S037938931730042X
Guías Clínicas
Se incluyen guías clínicas nacionales e internacionales consensuadas en el manejo de esta patología. ¿Cómo se estudia y etapifica el cáncer gástrico?, ¿Cómo se trata el cáncer gástrico?, ¿Existen algoritmos de manejo?.
- GES cáncer gástrico
http://www.supersalud.gob.cl/difusion/665/w3-article-601.html
- Guía japonesa 2014 cáncer gástrico
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5215069/
- NCCN cáncer gástrico
https://www.nccn.org/professionals/physician_gls/default.aspx#site
Linfadenectomía laparoscópica y preservación esplénica
- Preservación esplénica vs esplenectomía en cáncer gástrico laparoscópico Nuevo
https://www.ncbi.nlm.nih.gov/pubmed/28577727
Vídeos de técnicas quirúrgicas
- Este link te llevará a la pagina web de la SSAT (Sociedad de Cirugía del Tracto Alimentario)
http://ssat.com/video/gastric.cgi
Reacción Inmune Post Operatoria
- Reacción inmune post cirugía laparoscópica
https://www.ncbi.nlm.nih.gov/pubmed/18521842
- Reacción inmune post cirugia laparoscópica 2
https://www.ncbi.nlm.nih.gov/pubmed/20419322
Fístula de Muñón Duodenal
Te ofrezco 4 artículos que analizan esta difícil situación postoperatoria … Involucra pacientes en quienes se realizó una gastrectomía como parte del tratamiento del cáncer gástrico y evolucionaron con una fistula del muñón duodenal.
- Fístula duodenal I
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4773460/
- Fístula duodenal II
https://www.ncbi.nlm.nih.gov/pubmed/25491774
- Fístula duodenal III
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4481454/
- Fístula duodenal IV
https://www.ncbi.nlm.nih.gov/pubmed/24399492
Carcinoide Gástrico
- Esta revisión narrativa engloba el enfrentamiento del carcinoide gástrico
Omentoburdectomía en Cáncer Gástrico
¿Qué es la bursa?, ¿Qué es la omentectomía?, ¿Cuándo está indicado su resección en cáncer gástrico?, ¿Cuál es su fundamento fisiopatológico?.
- Omentobursectomía cáncer gástrico
http://www.scielo.cl/scielo.php?script=sci_arttext&pid=S0718-40262015000600016
Tratamiento en Cáncer Gástrico Metastásico
El tratamiento médico y/0 quirúrgico del cáncer gástrico se puede extender incluso en paciente etapa IV. En esta sección encontraras distintos artículos enfocados a terapia paliativa médica, terapia quirurgica en metástasis hepáticas, cirugía de citorreducción, quimioterapia intraoperatoria en carcinomatosis peritoneal y qué alternativas existen en el enfrentamiento de un paciente con cáncer gástrico perforado.
- Cáncer gástrico metastásico, enfrentamiento quirúrgico
https://www.ncbi.nlm.nih.gov/pubmed/22354489
https://www.ncbi.nlm.nih.gov/pubmed/24146196
https://www.ncbi.nlm.nih.gov/pubmed/20651395
- Cáncer gástrico metastásico enfrentamiento quimioterapéutico
https://www.ncbi.nlm.nih.gov/pubmed/23335104
- HIPEC cancer gastrico
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3471098/
- Enfrentamiento del cáncer gástrico perforado
https://www.ncbi.nlm.nih.gov/pubmed/24122093
Adyuvancia en Cáncer Gástrico
Podrás descargar un esquema resumen de adyuvancia en esta patología, formato ppt y jpg, que resumen la evidencia del consenso panamericano de cáncer gástrico del año 2016 y los artículos de esta sección del post.
Además encontrarás trials de adyuvancia en cáncer gástrico, tales como: MAGIC, MACDONALD, GYMSSA y REGATTA.
Complementariamente te ofrezco una revisión narrativa de otras terapias adyuvantes y un artículo con consideraciones respecto a quimio y radiopterapia en el tratamiento del cáncer gástrico desde el punto de vista de Cirujanos Digestivos.

- GYMSSA trial
https://www.ncbi.nlm.nih.gov/pubmed/20030854
- REGATTA trial
https://www.ncbi.nlm.nih.gov/pubmed/26822397
- Macdonald trial
http://www.nejm.org/doi/full/10.1056/NEJMoa010187#t=article
- MAGIC trial
http://www.nejm.org/doi/full/10.1056/NEJMoa055531
- Quimioterapia perioperatoria MAGIC y más.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4481429/
- Quimioterapia y/o radioterapia en pacientes con cáncer gástrico resecables o potencialmente curativos. Visión de cirujanos.
Soy paciente…
Si eres paciente y deseas saber más sobre tu enfermedad te recomiendo el siguiente link.
http://www.cancer.org/espanol/cancer/cancerdeestomago/si-usted-tiene-cancer-de-estomago
VIDEOS HCUCH
El siguiente video fue creado en la década de los 80 en el Hospital Clínico de la Universidad de Chile. Gracias al permiso del Director de Departamento de Cirugía, Dr. Julio Yarmuch, ha sido rescatado y re-editado para su difusión como testimonio histórico.
Se presenta una gastrectomía total abierta indicada en un paciente con cáncer gástrico cardial.
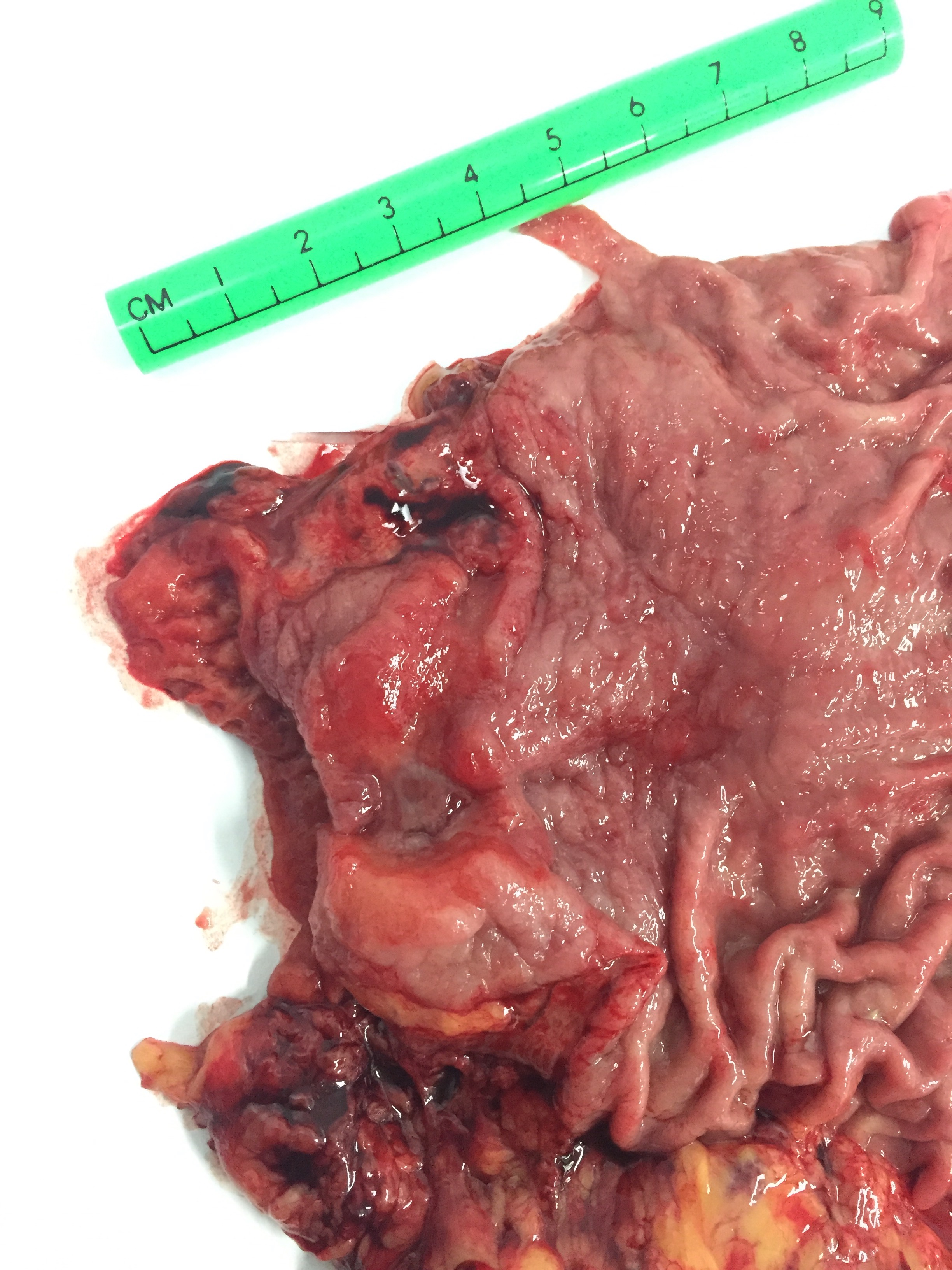





































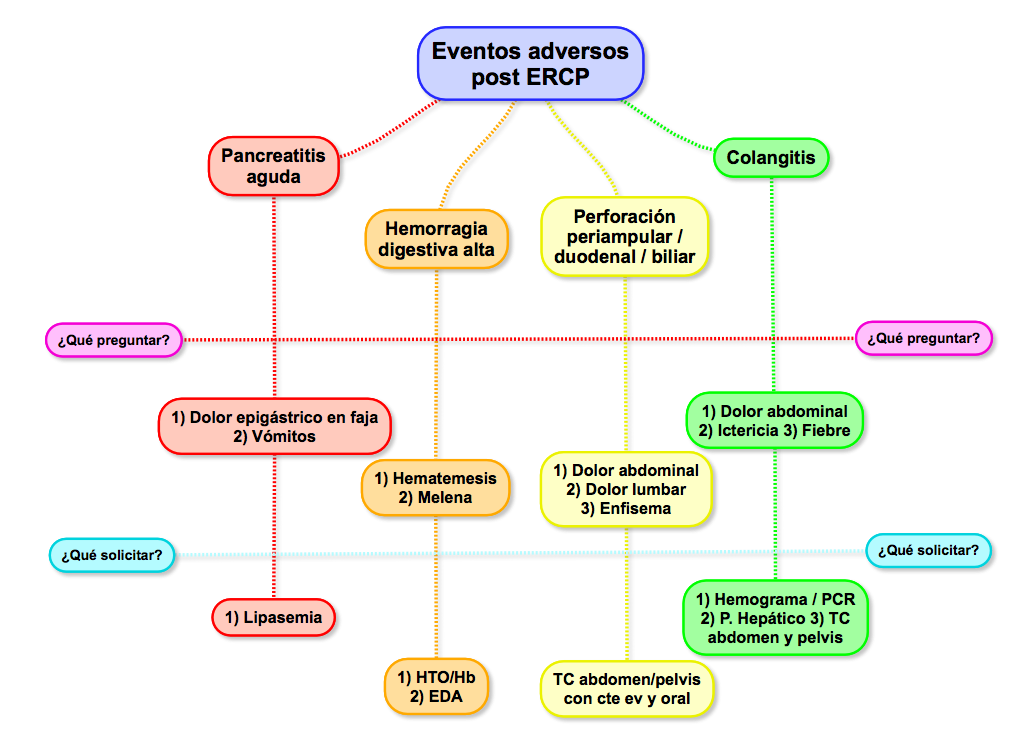













































































































 Factores de riesgo:
Factores de riesgo:








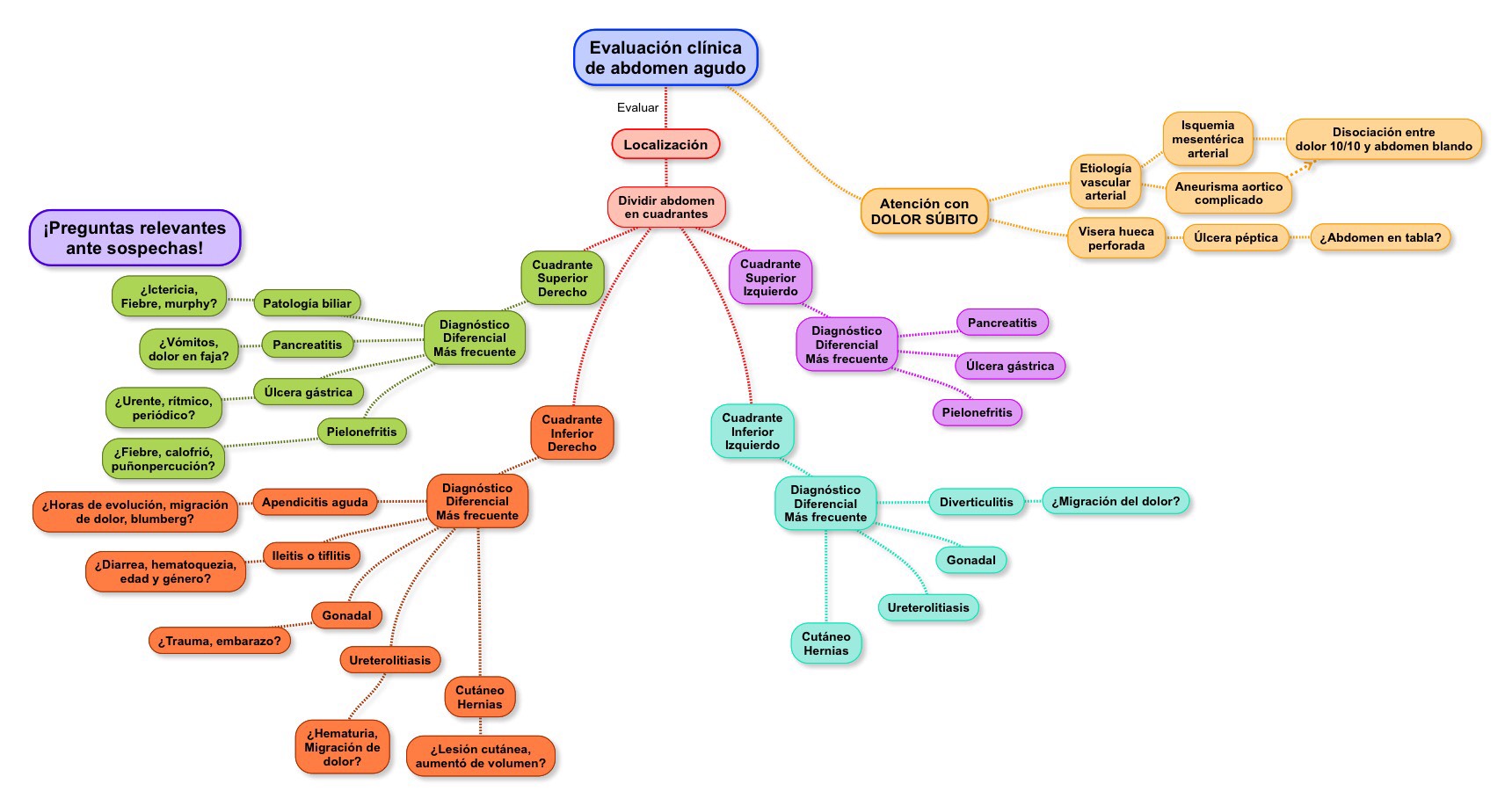

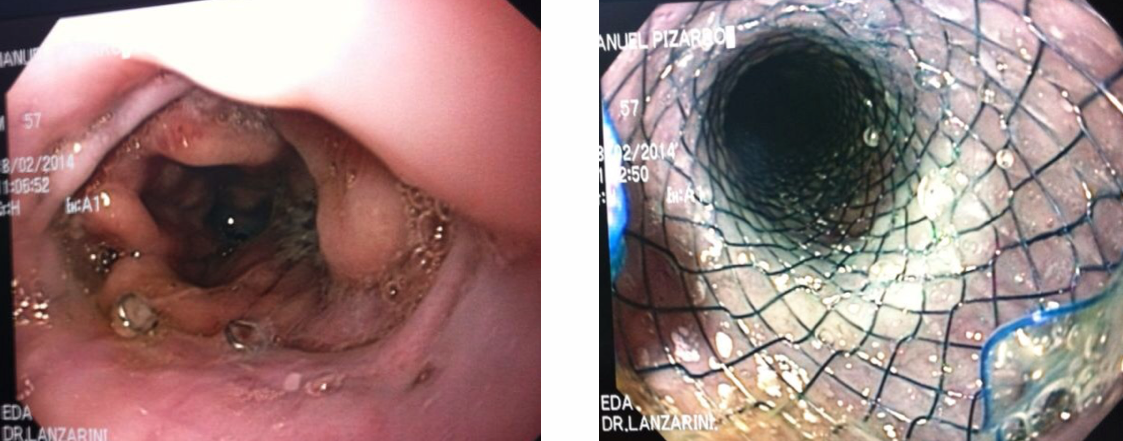


















Debe estar conectado para enviar un comentario.